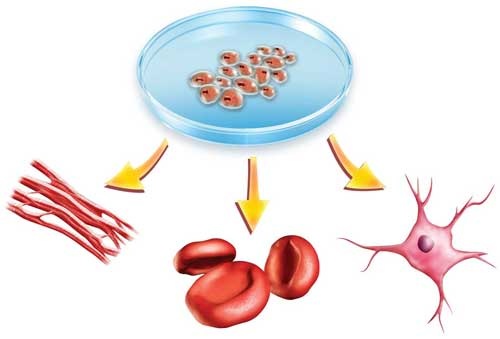
Implantes de células madre al corazón.
Las enfermedades cardiacas crónicas se distinguen por la pérdida irreversible de cardiomiocitos y, aun cuando se ha demostrado que el corazón posee actividad mitótica, se considera que esta es inadecuada y no detiene la progresión de las afecciones cardiovasculares crónicas hacia su etapa terminal.
La insuficiencia cardiaca tiene alta prevalencia en mayores de 65 años, y desde los 45 años se duplica cada década. Tiene una recurrencia de 65%, una mortalidad de 75% en hombres y 62% en mujeres, a 5 años. Esto toma gran relevancia en México, ya que la primera causa de muerte continua siendo las enfermedades del corazón.
La insuficiencia cardiaca tiene como principal causa a la cardiopatía isquémica.
La terapia celular para la regeneración miocárdica representa una gran oportunidad para crear nuevas estrategias.
El objetivo primario de dicha terapia consiste en optimizar y reorganizar áreas del corazón, en las cuales los cardiomiocitos han sido remplazados por tejido cicatricial, con células con potencial de biogénesis o angiogénesis, y restaurar la función en estas áreas funcionalmente perdidas (acinéticas).
Este objetivo podría alcanzarse mediante tres vías diferentes:
1.- Estimular los cardiomiocitos residuales a reentrar en un ciclo mitótico, (posibilidad que se está investigando y que en un futuro podría llevarse a cabo, pero en la actualidad todavía parece lejana).
2.- Terapia génica, consiste en transformar los fibroblastos de la cicatriz miocárdica en células contráctiles mediante transfección génica (todavía en fase experimental).
3.- implantar células, en la zona infartada, con el potencial de diferenciación (células madre) en cardiomiocitos potencialmente contráctiles o en nuevos vasos sanguíneos (angiogenesis). Esta alternativa es, por el momento, la más realista e investigada y la que ocupa este programa.
La insuficiencia cardiaca tiene alta prevalencia en mayores de 65 años, y desde los 45 años se duplica cada década. Tiene una recurrencia de 65%, una mortalidad de 75% en hombres y 62% en mujeres, a 5 años. Esto toma gran relevancia en México, ya que la primera causa de muerte continua siendo las enfermedades del corazón.
La insuficiencia cardiaca tiene como principal causa a la cardiopatía isquémica.
La terapia celular para la regeneración miocárdica representa una gran oportunidad para crear nuevas estrategias.
El objetivo primario de dicha terapia consiste en optimizar y reorganizar áreas del corazón, en las cuales los cardiomiocitos han sido remplazados por tejido cicatricial, con células con potencial de biogénesis o angiogénesis, y restaurar la función en estas áreas funcionalmente perdidas (acinéticas).
Este objetivo podría alcanzarse mediante tres vías diferentes:
1.- Estimular los cardiomiocitos residuales a reentrar en un ciclo mitótico, (posibilidad que se está investigando y que en un futuro podría llevarse a cabo, pero en la actualidad todavía parece lejana).
2.- Terapia génica, consiste en transformar los fibroblastos de la cicatriz miocárdica en células contráctiles mediante transfección génica (todavía en fase experimental).
3.- implantar células, en la zona infartada, con el potencial de diferenciación (células madre) en cardiomiocitos potencialmente contráctiles o en nuevos vasos sanguíneos (angiogenesis). Esta alternativa es, por el momento, la más realista e investigada y la que ocupa este programa.
Dos descubrimientos recientes revolucionaron la biología de las células madre.

1.- Se detectaron en órganos que se presumía carecían de potencial regenerativo, como el cerebro y los músculos. Se comprobó que varias aéreas del cerebro contienen células madre que mantienen su capacidad de proliferar y diferenciarse en los diferentes tipos de células neuronales. Las células del musculo esquelético (mioblastos) pueden cultivarse e implantarse en músculos receptores para reparar el daño tisular.
2.- Las células madre órgano-especificas del adulto parecen tener mucha mayor plasticidad de la que se creía. Se denomina plasticidad a la capacidad de las células madre presentes en un tejido adulto para generar tipo de células diferenciadas de otros tejidos, en su nueva localización.
Todos estos conocimientos brindan la esperanza de que ciertos tipos de células madre, como los cardiomiocitos fetales, células madre embrionarias, mioblastos o células satélite musculares, y células madre de la medula ósea, con las cuales ya se ha trabajado experimental o clínicamente, puedan utilizarse en la regeneración miocárdica.
Los cardiomiocitos fetales fueron las primeras células utilizadas para realizar una cardiomioplastía celular, parecen ser el tipo ideal para remplazar a los cardiomiocitos perdidos. Sin embargo tienen algunos obstáculos para su uso generalizado: posibilidad de rechazo, requieren de inmunosupresores y existen razones de carácter ético, son muy sensibles a la isquemia y mueren en gran cantidad (hasta 99%) al ser implantadas.
Las células madre embrionarias se desarrollan en el quinto día de la fertilización en el embrión humano en estado de blastocito. Su utilidad está limitada por su dificultad en el aislamiento, la posibilidad de rechazo, su propiedad de arritmogenesis y la posibilidad de crear tumores (teratocarcinomas) e implicaciones éticas, legales y religiosas, entre otras.
Las células madre de la medula ósea mantienen la capacidad de una ilimitada proliferación de células indiferenciadas, que pueden diferenciarse en distintos tipos celulares, que incluyen los cardiomiocitos. Pueden procurarse con facilidad, no tienen problemas éticos, ni de histocompatibilidad. Se evita la transmisión de virus u otros patógenos, ya que las células se obtienen del mismo paciente.
Las células de la medula ósea y de la sangre periférica contienen células endoteliales progenitoras, con capacidad de diferenciarse en nuevos vasos sanguíneos y cardiomiocitos en el tejido cardiaco cuando son implantadas directamente al miocardio.
Estos precursores hematopoyéticos se obtienen, en nuestro programa, de la sangre periférica por medio de citoferesis.
La forma de administrar las células madre a las aéreas lesionadas del corazón es fundamental para el éxito de la terapia celular, y para que ocurra, dichas áreas deben recibir una alta concentración de células madre y que estas no emigren a otras áreas. Las vías utilizadas son la intravenosa, intracoronaria, transendocárdica y la intramiocárdica.
La intravenosa es la mas fácil, pero su principal desventaja es que la células pasan por el filtro pulmonar antes de llegar al corazón, además de que las arterias coronarias solo reciben 3% del gasto cardiaco por minuto, lo que implica que las células madre deben sortear varias veces el paso por la circulación sistémica antes de poder llegar a las áreas lesionadas.
La administración por vía coronaria es sencilla, practica y tiene la ventaja de llevar las células al área lesionada y con regular concentración, pero no es sembrada en forma uniforme ni equitativa en las áreas que se requieren, porque además en las oclusiones coronarias crónicas, la perfusión es diferente en las distintas áreas que deben irrigar.
En el abordaje intramiocardico la inyección se realiza bajo visión directa, lo que permite, entre otras cosas, la identificación del área lesionada, y la concentración de las células madre es equilibrada, por lo que, a pesar de ser invasiva, se considera que es la mejor vía para administración de células madre al miocardio lesionado.
Los cardiomiocitos fetales fueron las primeras células utilizadas para realizar una cardiomioplastía celular, parecen ser el tipo ideal para remplazar a los cardiomiocitos perdidos. Sin embargo tienen algunos obstáculos para su uso generalizado: posibilidad de rechazo, requieren de inmunosupresores y existen razones de carácter ético, son muy sensibles a la isquemia y mueren en gran cantidad (hasta 99%) al ser implantadas.
Las células madre embrionarias se desarrollan en el quinto día de la fertilización en el embrión humano en estado de blastocito. Su utilidad está limitada por su dificultad en el aislamiento, la posibilidad de rechazo, su propiedad de arritmogenesis y la posibilidad de crear tumores (teratocarcinomas) e implicaciones éticas, legales y religiosas, entre otras.
Las células madre de la medula ósea mantienen la capacidad de una ilimitada proliferación de células indiferenciadas, que pueden diferenciarse en distintos tipos celulares, que incluyen los cardiomiocitos. Pueden procurarse con facilidad, no tienen problemas éticos, ni de histocompatibilidad. Se evita la transmisión de virus u otros patógenos, ya que las células se obtienen del mismo paciente.
Las células de la medula ósea y de la sangre periférica contienen células endoteliales progenitoras, con capacidad de diferenciarse en nuevos vasos sanguíneos y cardiomiocitos en el tejido cardiaco cuando son implantadas directamente al miocardio.
Estos precursores hematopoyéticos se obtienen, en nuestro programa, de la sangre periférica por medio de citoferesis.
La forma de administrar las células madre a las aéreas lesionadas del corazón es fundamental para el éxito de la terapia celular, y para que ocurra, dichas áreas deben recibir una alta concentración de células madre y que estas no emigren a otras áreas. Las vías utilizadas son la intravenosa, intracoronaria, transendocárdica y la intramiocárdica.
La intravenosa es la mas fácil, pero su principal desventaja es que la células pasan por el filtro pulmonar antes de llegar al corazón, además de que las arterias coronarias solo reciben 3% del gasto cardiaco por minuto, lo que implica que las células madre deben sortear varias veces el paso por la circulación sistémica antes de poder llegar a las áreas lesionadas.
La administración por vía coronaria es sencilla, practica y tiene la ventaja de llevar las células al área lesionada y con regular concentración, pero no es sembrada en forma uniforme ni equitativa en las áreas que se requieren, porque además en las oclusiones coronarias crónicas, la perfusión es diferente en las distintas áreas que deben irrigar.
En el abordaje intramiocardico la inyección se realiza bajo visión directa, lo que permite, entre otras cosas, la identificación del área lesionada, y la concentración de las células madre es equilibrada, por lo que, a pesar de ser invasiva, se considera que es la mejor vía para administración de células madre al miocardio lesionado.
Referencias Bibliográficas.
American Heart Association.Heart and stroke statistical update. Texas: American Heart Association, 2001.
Anversa P. Myocite death in the pathological heart. Circ Res 2000; 86: 121-23
Asahara T. Bone marrow origin of endothelial progenitor cells responsible for postnatal
vasculogenesis in physiological and pathological neovascularitation. Circ Res
1999;85:221.28
Beltrami P. Evidence that human cardiac myocite divide after myocardial infarction. N.
Engl J Med 2001; 344: 1750-62
Bristow MR. Drugs used in the treatment of heart failure. Braunwlad, editor. Heart Disease. Philadelphia:
WB Saunders, 2001: pp:562.
Garrido M. Reporte de mortalidad de los últimos 6 años de pacientes en espera de trasplante
de la clínica de insuficiencia cardiaca. Arch Inst Cardiol Mex 1999; 69 (suppl): 44.
Goldman SA. Neuronal production, migration and differentiation in a vocal control
nucleus of the adult female canary brain. Proc Natl acad Sci USA 1983;
80:2390-7.
Hassink RJ. Transplantation of cells for cardiac repair. J.Am.cell cardiol 2003; 41:711-17
Hughes S. Cardiac stem cells. J pathol 2002;197:468-78
Hyun-Jag K. Effects of intracoronary infusion of peripheral blood stem-cell mobilized
with granulocyte-colony stimulating factor on left ventricular systolic function
and restenosis after coronary stenting in myocardial infarctation. The magic
cell randomized clinical trial, Lancet 2004; 363;751-56
Implications of baseline ECG features and their serial changes in subjet with ventricular hypertrophy. Circulation 1994; 90: 1786-93
Kaji EH Gene and stem cell therapies. JAMA 2001;285:545-52
Kawamoto A. Therapeutic potencial of ex vivo expanded endothelial progenitor cells for myocardial
ischemia. Circulation 2001; 103:734-7
Kawamoto A. Intramyocardial transplantation
of autologous endothelial progenitor cells for therapeutic neovascularization of
myocardial ischemia. Circulation 2003;107:461-68
Louis AA. The heart protection study, IONA, CARISA, ENRICHID, ACUTE, ALIVE, MADIT II, and
REMATCH. Eur J Heart Fail 2002; 4: 11-35
Menasche P. Cardiac reparation: Fixing the heart with cells, new vessels and genes. Eur Heart J 2002; 4: D 73-78
Mezey E. Turning blood into brain: cells bearing neuronal antigens generated in vivo from bone narrow.
Science 2000;1779-82
Minami E. Skeletal muscle meets cardiac muscle. Friends or foes? J. Am Cardiol 2003; 41: 1084-86.
Nadal-Ginard B. Inducción de nuevos cardiomiocitos en el corazón adulto: futuro de la
regeneración miocárdica como alternativa de trasplante. Rev Esp Cardiol 2001; 54:543-50
National Heart Lung and Blood Institute: Morbidity and mortality chart book on cardiovascular, lung and
blood disease. 1990;NHLBI, Bethesda, 1992.
Orlic D. Stem cells for myocardial regeneration. Circ Res 2002; 991: 1092-102.
Orlic D. Purification and characterization of heterogenous pluripotent hematopoietic stem
cell populations expressing high levels of c-kit receptor. Blood 1993;82:762-80
Preston SL. The new stem cell biology: something for everyone. Mol pathol 2003; 56:86-98
Reyes M. Origin of endothelial progenitors in human postnatal bone marrow. J Clin Invest
2002; 109: 337-46
Stamm C. Autologous bone marrow stem cells transplantation for myocardial regeneration. Lancet 2003;
61:45-46
Simons M.Clinican trials in coronary angiogenesis; issues, problems, consensus. An expert panel sumary Circulation 2000;102:E73-86
Strave BE. Repair of infarcted myocardium by autologous intracoronary mononuclear bone
marrow cell transplantation in humans. Circulation 2002; 106: 1913-18
Straver E. Stem cells therapy in perspective. Circulation 2003; 107:929-34
Tol B. Autotransplantation using peripheral blood stem cells mobilized by cyclophosphamide. Bone Marrow Transplant 1989; 4: 595-96
Wang JS. Marrow estromal cells for cellular cardiomyoplasty: feasibility and potential
clinical adventages. J Thorac Cardiovasc Surg 2000; 120: 999-1005.
Zhang M. cardiomyocyte grafting of cardiac repair: graft cell death and antideath
strategies. J Mol Cell Cardiol 2001;33:907.